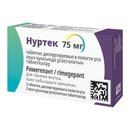
3 044.00
с учетом бонусов
3 541.00
3 807.00
-
+
Добавить в избранное
пр-т Красного Знамени, 86
3 044.00
с учетом бонусов
3 612.00
3 807.00
-
+
ул. Жигура, 48
3 044.00
с учетом бонусов
3 648.00
3 882.00
-
+
ул. Ладыгина, 7
3 044.00
с учетом бонусов
3 577.00
3 844.00
-
+
ул. Сахалинская, 41г
3 044.00
с учетом бонусов
3 541.00
3 807.00
-
+
Сообщить о неточности
Отправить сообщение